近日,核科学技术学院苗庆庆教授课题组在《J. Am. Chem. Soc.》上发表了关于双靶向分子用于靶向放射核素治疗和疾病激活蛋白降解的研究论文。该研究开发了一种新型双靶向分子探针,结合了前列腺特异性膜抗原(PSMA)介导的靶向放射核素治疗(TRT)和组织蛋白酶B(CTSB)激活的蛋白降解技术(PROTACs),用于前列腺癌的精准治疗,显著提高了治疗的靶向性和疗效。

图1:双靶向分子用于TRT和PROTACs联合治疗示意图。
在研究中,作者指出当前的PROTACs技术在癌症治疗中虽潜力巨大,但仍存在药代动力学和特异性不足等问题。为了解决这些问题,课题组设计了natLu /177Lu-P-A探针,该探针通过靶向PSMA受体确保药物精准递送至肿瘤,同时利用CTSB激活的PROTACs分子在肿瘤部位特异性降解BRD4蛋白。BRD4的降解抑制了其下游RAD51AP1蛋白的表达,削弱了肿瘤细胞的DNA损伤修复能力,从而增强了TRT的效果。
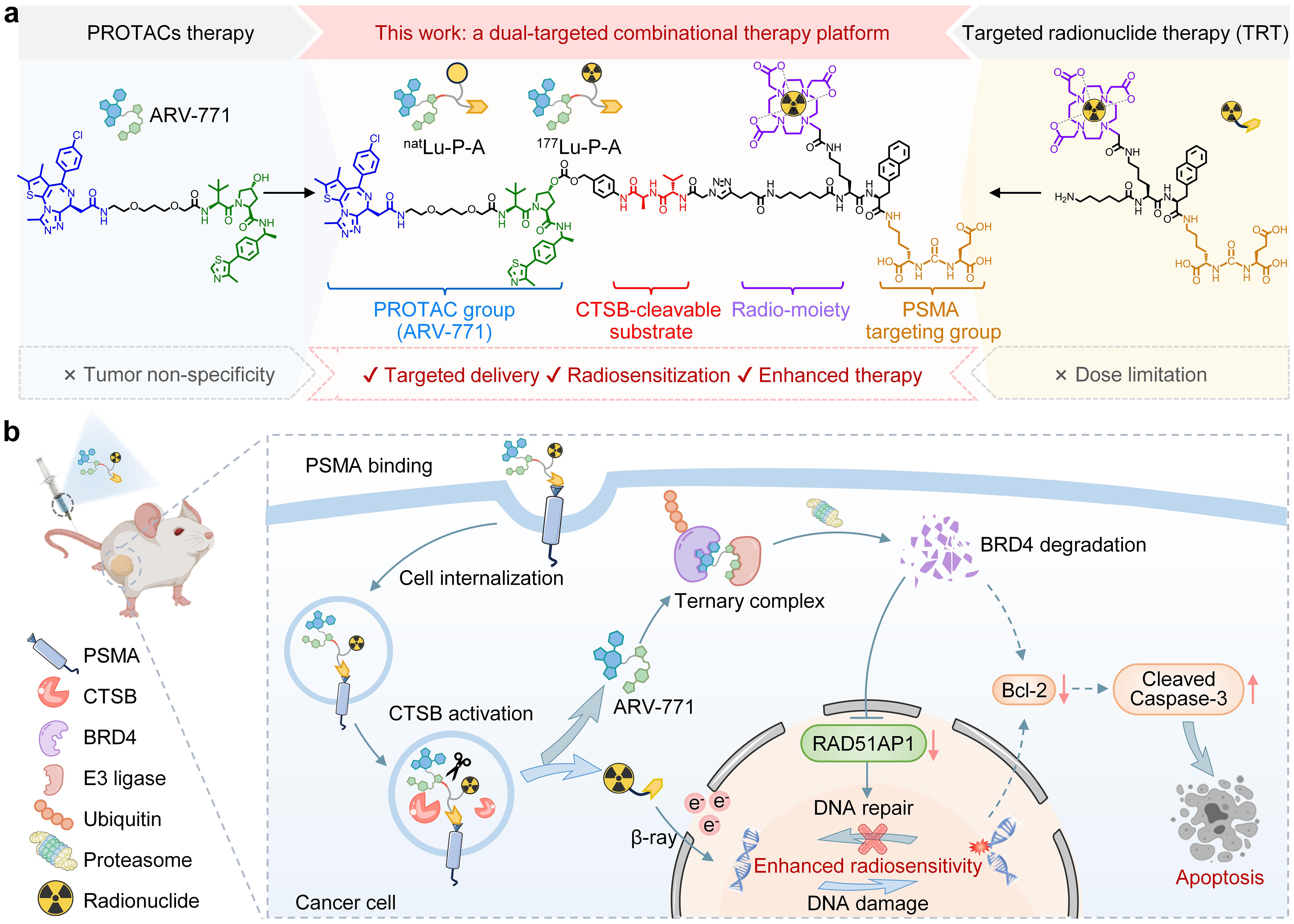
图2:TRT和PROTACs联合治疗前列腺癌的探针设计和双靶向探针示意图。
(a)177Lu-P-A的化学结构。(b)PSMA介导的TRT和CTSB激活的PROTACs联合治疗前列腺癌的示意图。
研究评估了双靶向探针natLu /177Lu-P-A在LNCaP肿瘤细胞和小鼠模型中的生物学活性,证明其具备优异的靶向性和特异性,与单一治疗相比, PROTACs和TRT的联合应用展现出更强的协同治疗效果。此外,探针表现出良好的药代动力学特性和肾脏清除率,表明其在临床应用中具有潜在价值。
该论文以“A Dual-Targeted Molecule for Disease-Activatable Proteolysis Targeting Chimeras and Targeted Radionuclide Therapy of Cancer”为题发表在权威期刊《J. Am. Chem. Soc.》(IF 14.5)上。该论文第一作者为课题组博士研究生张源,课题组硕士研究生顾维和博士研究生陈婉为论文共同第一作者,通讯作者为苗庆庆特任教授。该项研究得到了国家自然科学基金委等相关经费的支持。
论文链接:https://pubs.acs.org/doi/full/10.1021/jacs.4c18398
